О компьютерном подходе к решению расчетных химических задач
Вооружение учащихся знаниями и навыками использования современных ЭВМ в учебном процессе, на наш взгляд, один из наиболее. перспективных путей повышения эффективности обучения. Применение современных ЭВМ, в частности, при обучении химии не может сводиться лишь к ускорению расчетов. Оно должно быть направлено на более глубокое понимание учащимися изучаемых процессов и явлений.
Решение расчетных химических задач — первый этап применения ЭВМ в процессе обучения химии. Изучение количественных отношений в химии должно способствовать приобретению учащимися прочных знаний, развитию логического мышления при изучении химических явлений. Углубленное и четкое усвоение учащимися методики решения расчетных задач необходимо для более глубокого осмысливания теоретических положений, лежащих в основе расчетов.
Методика освоения задач каждого нового типа базируется на машинной логике и включает следующие этапы:
1) рассмотрение нескольких задач одного типа;
составление алгоритмов решения всех этих задач;
сравнительный анализ решений, выявление общего в составленных алгоритмах;
составление обобщенного алгоритма решения (при этом формулируются общие признаки, присущие данному типу задач);
5) составление программы вычислений для данного типа задач согласно обобщенному алгоритму.
В этой методике основное место отводится составлению алгоритма решения. Под алгоритмом, как известно, понимается последовательность точно сформулированных правил решения данной задачи. Алгоритм можно рассматривать: как план решения задачи.
В результате освоения каждого нового типа задач учащиеся составляют так называемую карту этого типа задач, содержащую обобщенный алгоритм, и, соответственно, программу вычислений. Эта карта содержит также контрольную задачу с ответом и с указанием времени автоматического выполнения программы. Приведем подробный пример составления одной из карт.
Название типа задач. Вычисление по химическому уравнению масс веществ по известной массе вещества (одного из вступающих или получающихся в результате реакции).
Условие (в общем виде): по уравнению химической реакции aA+6B=cC+dD вычислить массу вещества А (т*(А) г), необходимую для получения порции вещества С известной массы («'(С) г).
Составление алгоритма решения.
I. Нахождение исходных данных.
Так как по условию задачи надо определить массу одного вещества по известной массе другого вещества, для решения задач этого типа необходимо использовать соотношение m=vM где m — масса вещества (г), М — молярная масса вещества . (г/моль). Известно, что уравнение химической реакции выражает соотношение, числа молей веществ, участвующих и полученных, в. этой реакции, т. е. количества веществ V(A) и v(C), соответственно, прямо пропорциональны коэффициентам в уравнении реакции, отсюда v(A) моль=а, v(C) моль=с.
Анализируя химические формулы веществ А и С и используя таблицу относительных атомных масс, рассчитываем недостающие исходные данные: относительные молекулярные массы ЛТГ(А) и Afr(C), а так как численные значения относительных молекулярных и молярных масс равны, недостающими исходными данными будут: М(А) г/моль=Л7г(А),. Л1(С) г/моль=Л(г(С).
Используя исходные данные, приступаем к составлению алгоритма решения.

Программа вычислений (составляется согласно алгоритму решения).
Для удобства работы программа оформлена в виде табл. 1, рядом указано, в каких регистрах памяти хранятся исходные данные и результаты промежуточных вычислений. Приведенная программа имеет девять шагов.
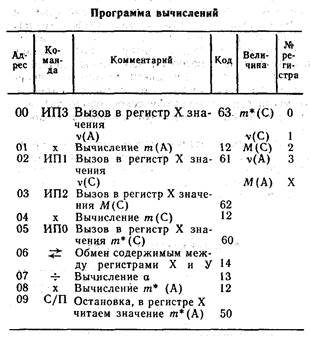
В левом столбце таблицы указан номер (адрес) шага, в среднем столбце проставлена последовательность команд, составляющих содержание программы, в правом столбце содержатся пояснения, раскрывающие смысл и назначение каждой команды (комментарий).
Контрольная задача (позволяет убедиться в отсутствии ошибок в программе).
Исходя из уравнения химической реакции СаО+Н20=Са(ОН)2, вычислить массу оксида кальция, необходимую для получения гидроксида кальция массой 37 г.
Заносим исходные данные в регистры памяти (табл. 2).
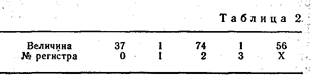
Время автоматического выполнения программы — 5 с.
Ответ: 28, следовательно, масса оксида кальция равна 28 г.
Таким образом мы составляем пакет карт для решения задач разных типов (сейчас в литературе для этого используется термин «пакет прикладных программ»).
Использование калькуляторов только для выполнения арифметических действий при решении расчетных химических задач, конечно, может решить на первый взгляд целый ряд проблем, например на первом этапе у учащихся повышается интерес к задачам, учитель имеет возможность экономить время урока. Однако если компьютеризацию рассматривать только в этом плане, т. е. использовать калькуляторы только для расчетов, не обращая серьезного внимания на алгоритм решения задачи, то такое применение калькуляторов на уроках химии может оказаться даже вредным с точки зрения освоения предмета.
Информация по педагогике:
Опоры необходимые для понимания
текста
Проблема использования опор при обучении чтению текстов на иностранном языке не является новой. В данной статье рассматриваются вопросы: сущность опор при чтении, виды опор при чтении; обучение учащихся старших классов базового уровня поиску опор при чтении текстов на английском языке. Применительн ...
Математическая игра как форма внеклассной работы по математике
На сегодняшний день существуют различные формы проведения внеклассной работы по математике с учащимися. К ним можно отнести: Математический кружок; Школьный математический вечер; Математическая олимпиада; Математическая игра; Школьная математическая печать; Математическая экскурсия; Математические ...
О
компьютерном подходе к решению расчетных химических задач
Вооружение учащихся знаниями и навыками использования современных ЭВМ в учебном процессе, на наш взгляд, один из наиболее. перспективных путей повышения эффективности обучения. Применение современных ЭВМ, в частности, при обучении химии не может сводиться лишь к ускорению расчетов. Оно должно быть ...
Дистанционное обучение

Дистанционную форму обучения специалисты по стратегическим проблемам образования называют образовательной системой 21 века.
Навигация
- Главная
- Интенсивная школа
- Болонский процесс
- Методы физического воспитания
- Обучение как процесс
- Воспитание в детских дошкольных учреждениях
- Факторы, влияющие на развитие ребенка
- Другая информация
